研究领域:癌症遗传学、基因组稳定性、DNA损伤与修复机制
基因组的稳定性对生物的遗传特征以及防止肿瘤的发生是及其重要的。一个健康的细胞如果要最终转变为癌细胞,必须获得特异的基因突变和表观遗传改变,才能使其分裂不受限制,逃避凋亡和免疫监视,进行代谢重编程,并减少对生长因子的依赖,等等。导致产生恶性细胞的基因突变中,DNA损伤应答机制的缺陷是最早出现的和常见的,Li Lab的研究旨在了解DNA损伤如何导致突变的发生,以及基因组不稳定性如何导致癌症。目前,课题组的研究方向主要包括以下三个方面:
范可尼贫血症的分子机制及发病机理
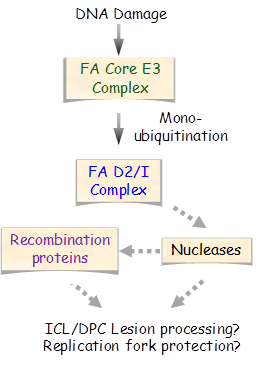
范可尼贫血症(Fanconi anemia, FA)的临床症状包括渐进性贫血, 渐进性骨髓衰竭,染色体异常和极强的肿瘤易感性。FA患者细胞的特征则反映DNA交联损伤修复能力的严重缺陷。范可尼贫血患者的细胞对DNA交联剂高度敏感,使得这一遗传病成为研究复杂型DNA损伤的主要模型。尽管目前在患者中发现了24种FA基因的遗传缺失与范可尼贫血直接相关,但范可尼贫血通路功能在DNA损伤修复和缓解复制压力的分子机制仍然有待阐明。1. 范可尼贫血途径的遗传框架是什么?2. DNA-蛋白质交联(DPC)损伤是否范可尼贫血症的致病损伤?3. 为什么范可尼贫血通路的缺陷会导致独特的全血性贫血和骨髓衰竭表型,而很少涉及其他组织器官?实验室近期的研究项目旨在回答这些问题,并从分子机制上深入了解这一复杂途径如何维护人类基因组的稳定性.
(Shen et al, Molecular Cell, Vol. 80, Dec., 17 2020)
DNA修复缺陷的补偿机制
每一个DNA修复通路的遗传缺陷会导致特异的疾病表型,以及细胞对特定类型DNA损伤剂的超敏反应。然而,大部分 DNA修复功能的缺陷在没有外源损伤的条件下不导致细胞死亡。尽管细胞内源性DNA损伤在不断发生,整体遗传性缺陷导致的范可尼贫血症、着色性干皮病、碱基错配修复综合征患者大部分能存活至青少年或成年期。这表明细胞中存在代偿机制 (Compensatory Pathways),可以阻止DNA修复缺陷细胞积累大量的DNA损伤而致死。 我们通过全基因组合成致死的筛选方法在DNA修复缺陷细胞中找到并分析这些补偿机制。识别各种DNA修复缺陷的补偿机制有助于建立新型的癌症治疗靶点,尤其是由DNA损伤修复缺陷引发的肿瘤.
(R Wang et al, Proceedings of the National Academy of Science, USA, PMID:33376220. June, 2021)
DNA 蛋白质交联 (DPC)损伤的修复

DNA-蛋白质交联(DNA-protein crosslink, DPC)是碱基和蛋白分子共价结合后的异常结构。这一类损伤结构对DNA复制和基因转录有无法跨越的阻断性。DPC是一种常见的DNA损伤。 电离辐射、DNA交联剂(例如甲醛)。以及常用于癌症治疗的双功能烷化剂都会引发DPC。PARP抑制剂、阿霉素、依托泊苷,顺铂等癌症化疗药物都可诱导DNA-蛋白质交联损伤。然而,对于DPC损伤修复的分子机制的了解目前相当有限。缺少遗传模型以及有效的检测方法等都是深入了解这一重要DNA损伤的障碍.
其他类型的DNA损伤相比,DPC的特征是蛋白质加合体的庞大性。导致蛋白因子功能在DPC损伤识别和修复过程中面临严重的空间阻碍。在细胞中,这一阻碍可以通过蛋白酶体或蛋白酶降解来减小蛋白加合物体积,将DPC上的蛋白转化为短肽加合物。短肽-DNA交联可能是NER(核酸剪切修复)通路的底物,也可由跨损伤DNA合成的途径保证DNA复制的连续性。另一方面,较大的蛋白酶解中间体,例如三级结构仍然保持的蛋白酶解中间产物,依旧对DNA转录及复制形成较强的阻碍,需要FA通路来清除。我们的工作将以DPC形成和修复机制作为主要目标之一.
(Q Hu et al., Cell Reports 30, 1235–1245, January 28, 2020)